
MutaSight
La Modélisation Moléculaire appliquée à l'Oncologie de Précision
Découvrez comment la modélisation moléculaire et les outils de bioinformatique révolutionnent le traitement du cancer en permettant une analyse précise des mutations tumorales.

Qu'est-ce que l'oncologie de précision ?
1. Diagnostic Avancé
Des analyses moléculaires approfondies permettent d'identifier les mutations responsables du développement tumoral pour mieux les cibler.
2. Thérapies Ciblées
L'oncologie de précision vise à développer des traitements spécifiques à chaque patient en se basant sur le profil génétique de sa tumeur.
3. Impact Clinique
Cette approche personnalisée améliore l'efficacité des traitements et réduit les effets indésirables.
Qu'est-ce qu'une mutation ?
1. Altération Génétique
Une mutation est un changement dans la séquence d'ADN d'un gène. Dans certains cas, elle peut mener au développement d'un cancer.
2. Impact Biologique
Selon le type et la localisation de la mutation, elle peut activer des oncogènes ou inactiver des gènes suppresseurs de tumeur.
3. Identification des Cibles
L'analyse des mutations aide à déterminer les meilleures options thérapeutiques pour chaque patient atteint de cancer.
La Modélisation Moléculaire au Service de l'Oncologie de Précision

Analyse de Séquences
En analysant les différences de séquence entre les protéines saines et les protéines mutées, les chercheurs peuvent détecter les anomalies qui contribuent au développement du cancer.
Modélisation Moléculaire
En modélisant l'impact des mutations identifiées, mais inconnues des bases de données, nous pouvons évaluer comment ces changements affectent la structure et la fonction des protéines. Ces analyses 3D révèlent comment les mutations déstabilisent ou modifient potentiellement la conformation des protéines, perturbant ainsi leurs interactions et leur activité.
Améliorer la prise en charge
En identifiant les protéines clés affectées par les mutations, les oncologues peuvent proposer à leur patient un traitement ciblé qui bloque spécifiquement leur activité.
La modélisation moléculaire en action
Le cas d'un patient atteint d'un mélanome uvéal qui a répondu au traitement proposé par son oncologue, basé sur les résultats d'analyse de Modélisation Moléculaire de mutations tumorales.
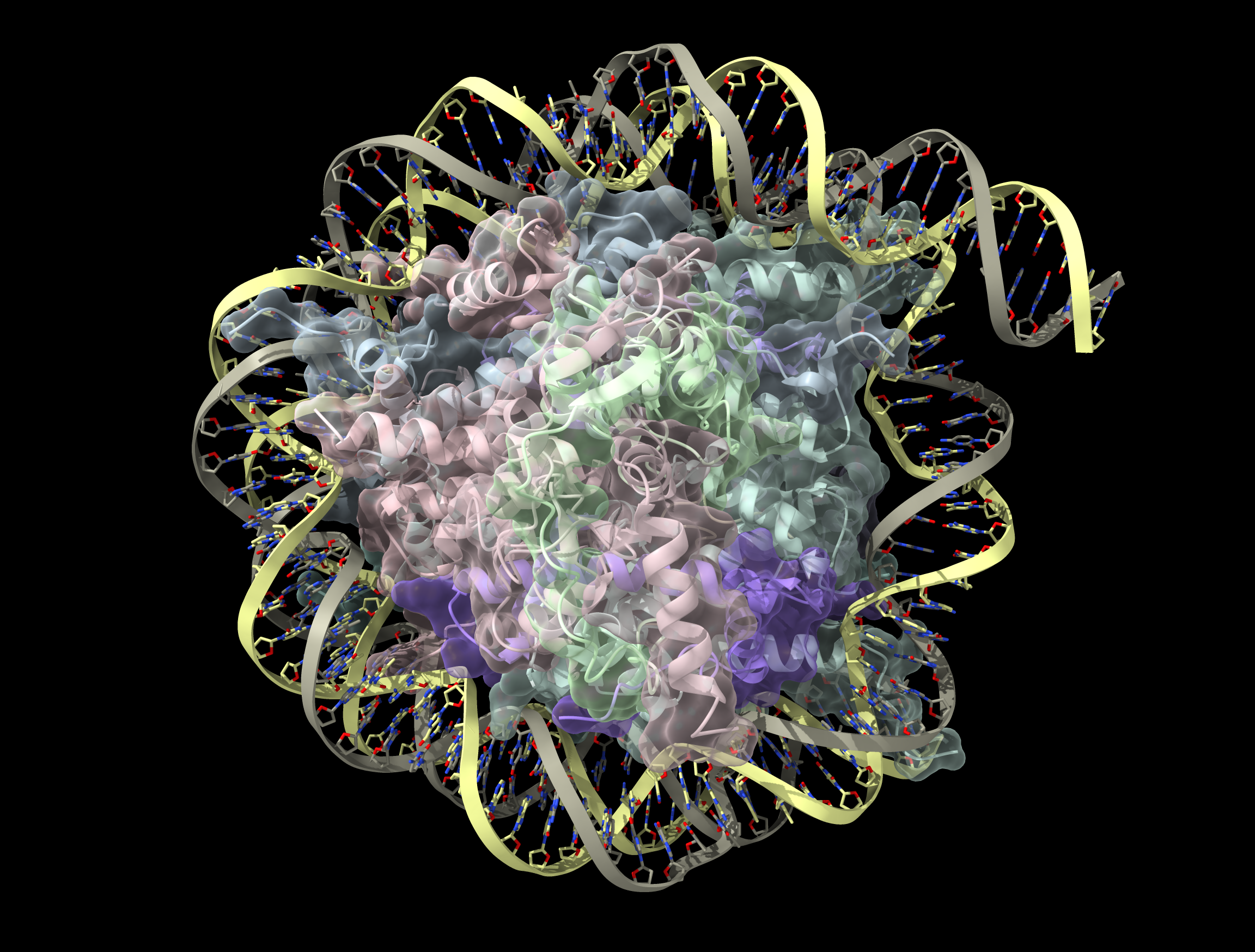
Analyses NGS
L'analyse Next-Generation Sequencing (NGS) de la biopsie d'un patient atteint d'un mélanome uvéal a détecté plusieurs mutations somatiques, dont certaines inconnues des bases de données.
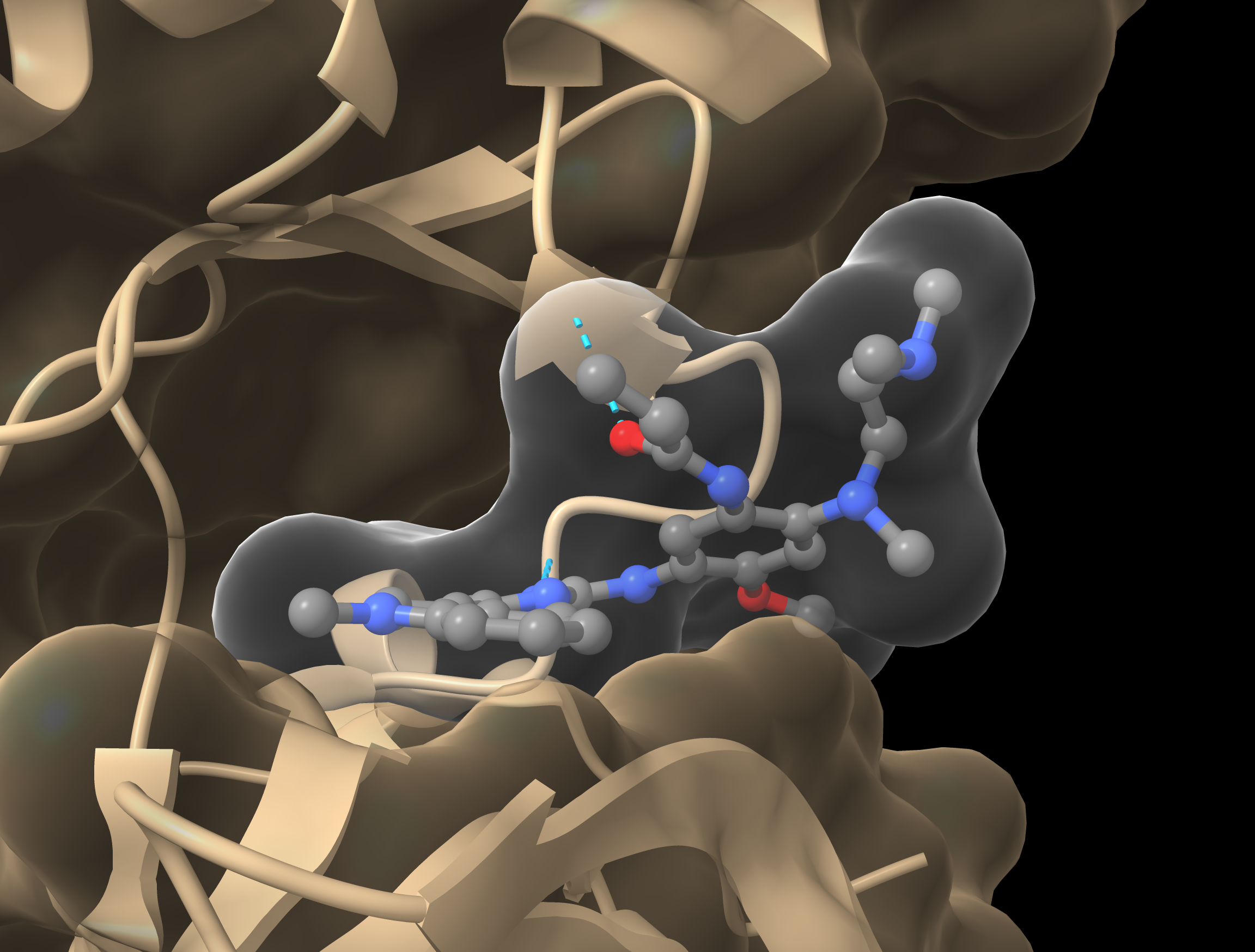
Analyse de Modélisation Moléculaire
L'analyse par Modélisation Moléculaire des mutations inconnues a prédit que deux d’entre elles pourraient être activatrices.
Décision Médicale
En s’inspirant des prédictions de la Modélisation Moléculaire, l'oncologue a proposé un traitement personnalisé pour son patient, qui montra une réponse à ce traitement.
Les détails de cette analyse ont été publiés dans une revue scientifique disponible via ce
lien
Trametinib Induces the Stabilization of a Dual GNAQ p.Gly48Leu- and FGFR4
p.Cys172Gly-Mutated Uveal Melanoma. The Role of Molecular Modelling in Personalized Oncology
Fanny S. Krebs et al. Int. J. Mol. Sci. 2020, 21, 8021.
Abstract. We report a case of an uveal melanoma patient with GNAQ p.Gly48Leu who responded to MEK inhibition. At the time of the molecular analysis, the pathogenicity of the mutation was unknown. A tridimensional structural analysis showed that Gαq can adopt active and inactive conformations that lead to substantial changes, involving three important switch regions. Our molecular modelling study predicted that GNAQ p.Gly48Leu introduces new favorable interactions in its active conformation, whereas little or no impact is expected in its inactive form. This strongly suggests that GNAQ p.Gly48Leu is a possible tumor-activating driver mutation, consequently triggering the MEK pathway. In addition, we also found an FGFR4 p.Cys172Gly mutation, which was predicted by molecular modelling analysis to lead to a gain of function by impacting the Ig-like domain 2 folding, which is involved in FGF binding and increases the stability of the homodimer. Based on these analyses, the patient received the MEK inhibitor trametinib with a lasting clinical benefit. This work highlights the importance of molecular modelling for personalized oncology.
