
MutaSight
Modellazione molecolare applicata all’oncologia di precisione
Scopri come gli strumenti di modellazione molecolare e bioinformatica stanno rivoluzionando il trattamento del cancro, consentendo un’analisi precisa delle mutazioni tumorali.


Scopri come gli strumenti di modellazione molecolare e bioinformatica stanno rivoluzionando il trattamento del cancro, consentendo un’analisi precisa delle mutazioni tumorali.

Di fronte al cancro possono sorgere molte domande, spesso senza risposte chiare o accessibili. Le informazioni disponibili sono talvolta complesse o difficili da comprendere. Ecco alcuni concetti chiave per aiutarvi a comprendere meglio questa malattia.
È caratterizzato da una proliferazione anomala di cellule in un tessuto. Ogni cancro è unico a causa delle sue specificità molecolari, anche tra due persone con lo stesso tipo di cancro.
È un ammasso di cellule derivante dalla proliferazione anomala di una cellula cancerosa. Può contenere miliardi di cellule. A volte alcune si staccano e invadono altre parti del corpo, formando metastasi.
È una modifica in una sequenza di DNA, il portatore delle nostre informazioni genetiche. Alcune mutazioni possono alterare la funzione cellulare, portando a comportamenti anomali o patologici.
Grazie ad analisi avanzate, i medici possono rilevare le mutazioni responsabili dello sviluppo del cancro e focalizzare il trattamento su questi bersagli.
L’oncologia di precisione punta a offrire trattamenti personalizzati, mirati alle caratteristiche specifiche del tumore di ogni paziente.
Le analisi avanzate permettono di individuare le mutazioni che favoriscono lo sviluppo del cancro e di intervenire miratamente.
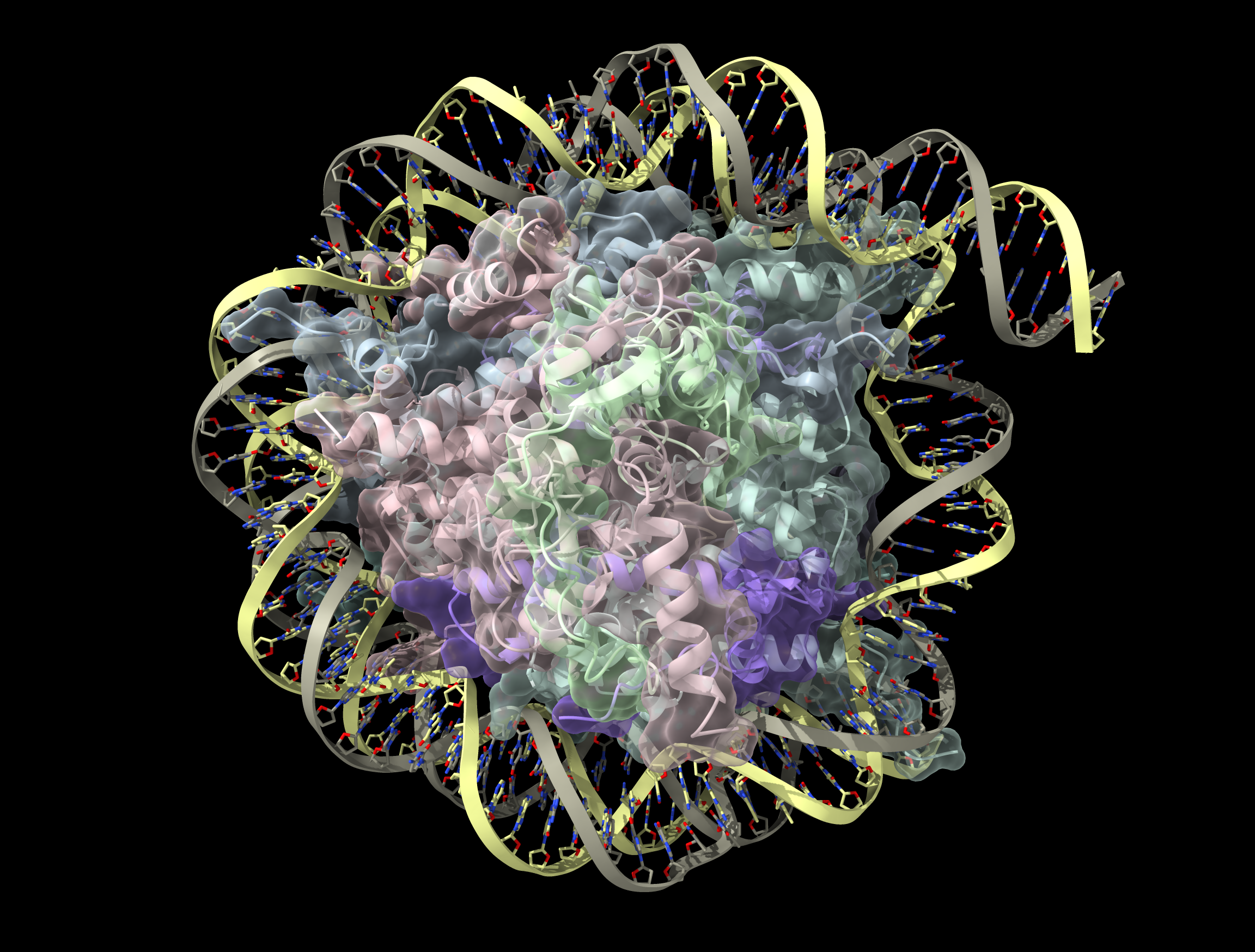
Una proteina è una molecola gigante composta da una successione di amminoacidi, i mattoni fondamentali della vita. Svolge funzioni essenziali nel corpo come la riparazione cellulare, la regolazione dei processi biologici o la difesa contro le infezioni.
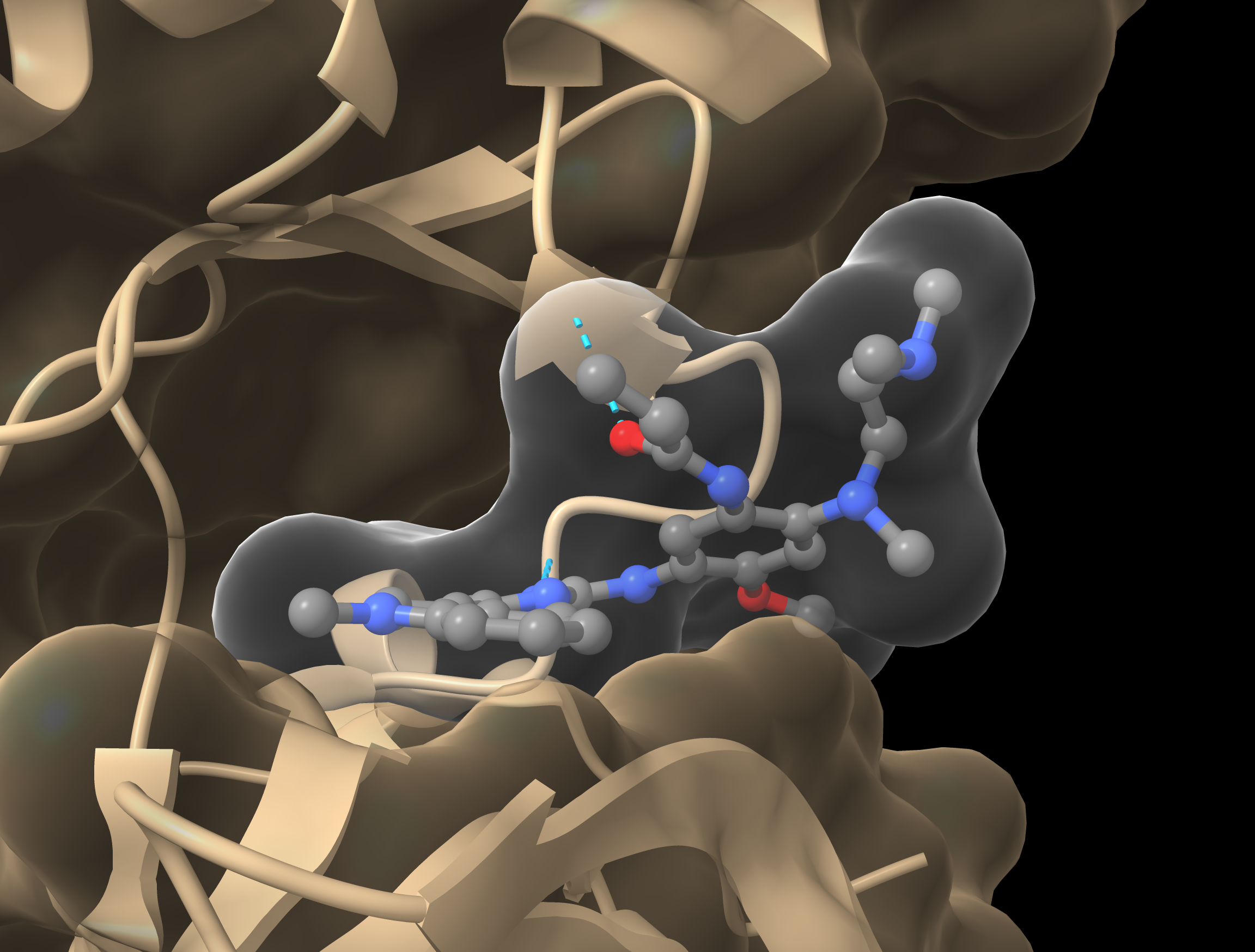
La modellazione molecolare è un metodo computazionale utilizzato per comprendere come proteine e altre molecole, come i farmaci, interagiscono tra loro.
Una mutazione può alterare il numero e la sequenza di amminoacidi di una proteina. Grazie ad analisi strutturali, possiamo prevedere gli effetti di tali cambiamenti sulla forma, funzione e capacità della proteina di interagire con altre molecole, come i farmaci.
Prendiamo l'esempio di un paziente affetto da un cancro raro e aggressivo che si è sviluppato nelle cellule pigmentate dell'occhio: il melanoma uveale. Questo tumore non rispondeva adeguatamente ai trattamenti standard, il che ha spinto l'oncologo curante a presentare il suo caso in un simposio professionale, il TumorBoard Moléculaire (TBM). Questo comitato riunisce esperti di diversi settori (oncologi, patologi, bioinformatici, genetisti, ecc.) per discutere casi complessi.
Prima di questo incontro erano state effettuate le analisi genetiche del tumore, che avevano rivelato la presenza di mutazioni nelle cellule tumorali sconosciute alla letteratura scientifica. Comprendere l’impatto di queste mutazioni potrebbe aiutare a guidare le scelte terapeutiche. Pertanto è stata effettuata un'analisi del modello molecolare per prevedere i possibili effetti di queste mutazioni sul comportamento delle proteine e quindi delle cellule. I risultati hanno mostrato che è probabile che queste mutazioni causino un comportamento cellulare anomalo e quindi promuovano la diffusione del cancro. Sulla base di queste analisi, l'oncologo è stato in grado di proporre un trattamento personalizzato che mira specificamente alle anomalie riscontrate nel tumore, portando ad effetti positivi per il paziente e ad un miglioramento delle sue condizioni.
I dettagli di questa analisi sono stati pubblicati su una rivista scientifica disponibile tramite questo
link
Trametinib Induces the Stabilization of a Dual GNAQ p.Gly48Leu- and FGFR4
p.Cys172Gly-Mutated Uveal Melanoma. The Role of Molecular Modelling in Personalized Oncology
Fanny S. Krebs et al. Int. J. Mol. Sci. 2020, 21, 8021.
Abstract. We report a case of an uveal melanoma patient with GNAQ p.Gly48Leu who responded to MEK inhibition. At the time of the molecular analysis, the pathogenicity of the mutation was unknown. A tridimensional structural analysis showed that Gαq can adopt active and inactive conformations that lead to substantial changes, involving three important switch regions. Our molecular modelling study predicted that GNAQ p.Gly48Leu introduces new favorable interactions in its active conformation, whereas little or no impact is expected in its inactive form. This strongly suggests that GNAQ p.Gly48Leu is a possible tumor-activating driver mutation, consequently triggering the MEK pathway. In addition, we also found an FGFR4 p.Cys172Gly mutation, which was predicted by molecular modelling analysis to lead to a gain of function by impacting the Ig-like domain 2 folding, which is involved in FGF binding and increases the stability of the homodimer. Based on these analyses, the patient received the MEK inhibitor trametinib with a lasting clinical benefit. This work highlights the importance of molecular modelling for personalized oncology.